Cell子刊:新研究利用CRISPR-Cas9成功地对人单核细胞进行基因编辑
来源:本站原创 2021-05-22 13:09
2021年5月22日讯/生物谷BIOON/---自CRISPR-Cas9基因编辑技术问世以来的十年间,科学家们已经利用该技术剔除或改变了越来越多的细胞类型中的基因。如今,在一项新的研究中,来自美国格拉德斯通研究所和加州大学旧金山分校的研究人员将人类单核细胞---在免疫系统中发挥关键作用的白细胞---添加到了这一列表中。他们将CRISPR-Cas9应用于单核细
2021年5月22日讯/生物谷BIOON/---自CRISPR-Cas9基因编辑技术问世以来的十年间,科学家们已经利用该技术剔除或改变了越来越多的细胞类型中的基因。如今,在一项新的研究中,来自美国格拉德斯通研究所和加州大学旧金山分校的研究人员将人类单核细胞---在免疫系统中发挥关键作用的白细胞---添加到了这一列表中。他们将CRISPR-Cas9应用于单核细胞,并展示了这种技术对了解人类免疫系统如何对抗病毒和细菌的潜在价值。这种技术为鉴定出对单核细胞功能最重要的人类基因以及针对一系列病原体提出新的治疗策略打开了大门,也为更多关于主要传染病和人类免疫细胞之间相互作用的研究奠定了基础。
相关研究结果发表在2021年5月11日的Cell Reports期刊上,论文标题为“Efficient generation of isogenic primary human myeloid cells using CRISPR-Cas9 ribonucleoproteins”。

单核细胞是免疫细胞,在保卫人体免受病原体侵害方面具有广泛的作用。作为其正常功能的一部分,单核细胞可以产生另外两种免疫细胞类型:巨噬细胞和树突细胞,前者吞噬并摧毁体内的外来物,后者帮助识别病原体并触发更具特异性的免疫反应。
这些作者以前利用CRISPR-Cas9技术研究过一种不同类型的称为T细胞的免疫细胞,以便选择性地去除这些细胞中的基因并观察其后果。他们的研究结果为新的免疫疗法指明了治疗靶点,使T细胞更有效地对抗疾病。
然而,单核细胞是出了名地难以在实验室中研究。很少有单核细胞在血液中循环,而且它们在培养皿中的行为与它们在体内的行为不同。因此,将CRISPR-Cas9应用于单核细胞需要调整标准实验过程。这些作者必须开发一种不仅要改变单核细胞内的基因还要确保这些被编辑的细胞仍有功能的方法。编辑单核细胞具有挑战性,但是他们认为在其他免疫细胞中复制他们在T细胞上取得的成功非常重要。
这些作者发现,用他们基于CRISPR的方法编辑的单核细胞仍然可以产生巨噬细胞和树突细胞。为了证实这些新编辑的细胞是否表现正常,他们用导致结核病的细菌感染了实验室里生长的细胞。他们发现,源自编辑过的单核细胞的巨噬细胞仍有能力吞噬这种病体。
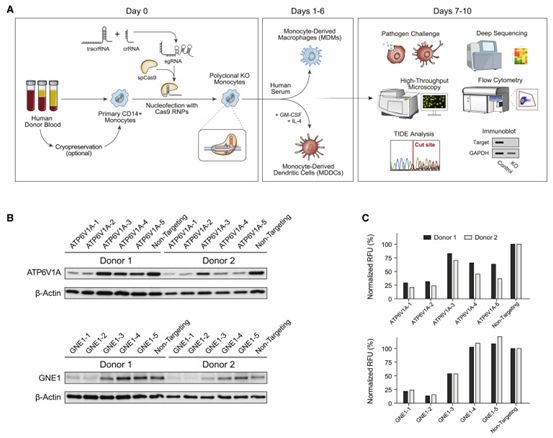
对人类髓系细胞进行CRISPR编辑的灵活平台,图片来自Cell Reports, 2021, doi:10.1016/j.celrep.2021.109105。
这些作者接下来发现,使用CRISPR-Cas9去除单核细胞中的基因SAMHD1---因此也去除所产生的巨噬细胞--使得这些细胞被HIV感染的几率提高了50倍以上。虽然已知SAMHD1可以保护人类细胞免受HIV感染,但该实验证实了他们在单核细胞中的基因编辑方法的成功,以及它在研究疾病方面的前景。
这些作者近年来一直在对病毒用来感染细胞和进行传播的人类蛋白进行编目。他们的研究已涵盖靶向巨噬细胞和树突细胞的HIV、结核杆菌、埃博拉病毒和登革热病毒。编辑这些细胞中的基因的新能力将帮助他们验证他们的发现,并确定可能有助于在未来对抗这些疾病的弱点。它也可能指向帮助提高单核细胞对抗感染能力的药物靶标,或者从一开始阻止病毒劫持单核细胞。
综上所述,鉴于这些作者确信他们可以成功地编辑单核细胞,他们的方法将使得他们能够深入地研究这些细胞,并了解它们在传染病中的作用。(生物谷 Bioon.com)
参考资料:
Joseph Hiatt et al. Efficient generation of isogenic primary human myeloid cells using CRISPR-Cas9 ribonucleoproteins. Cell Reports, 2021, doi:10.1016/j.celrep.2021.109105.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


