再获批!超过95%难治性癌症患者获得缓解,百时美施贵宝CAR-T疗法再获FDA批准
024年5月16日,美国FDA宣布,加速批准百时美施贵宝的CAR-T疗法扩展适应症,用于治疗复发/难治性滤泡性淋巴瘤(FL)成人患者,他们已经接受过两种及以上前期系统治疗。
94%患者肿瘤实现完全缓解!FDA批准BMS的CAR-T细胞疗法一项新适应症
该研究是一项全球性、多中心、开放标签、单臂、II期临床试验,共纳入了130例至少接受过二线治疗的复发或难治性惰性B细胞非霍奇金淋巴瘤患者。
FDA接受O药皮下注射剂型上市申请,有望明年初上市
纳武利尤单抗皮下注射制剂由纳武利尤单抗与Halozyme专有的重组人透明质酸酶PH20(rHuPH20)组成。
二十多年来首个!FDA批准非复杂性尿路感染新抗生素上市
3项对照研究评估了Pivya对比一种口服抗菌药物、布洛芬以及安慰剂的疗效,主要终点是综合反应率,包括临床治愈率和微生物学应答率。
FDA批准“减肥神药”司美格鲁肽用于预防心脏病,可显著降低肥胖者主要心血管不良事件风险
在接受司美格鲁肽治疗的肥胖的射血分数保留的心力衰竭患者中,体重减轻幅度越大,心力衰竭相关症状改善越明显。
缓解率69%!FDA加速批准百济神州BRUKINSA,用于治疗复发或难治性滤泡性淋巴瘤
BRUKINSA是迄今为止唯一一种对这种恶性肿瘤显示疗效的BTK抑制剂,目前在全球同类药物中拥有最广泛的标签,包括五种肿瘤学适应症。
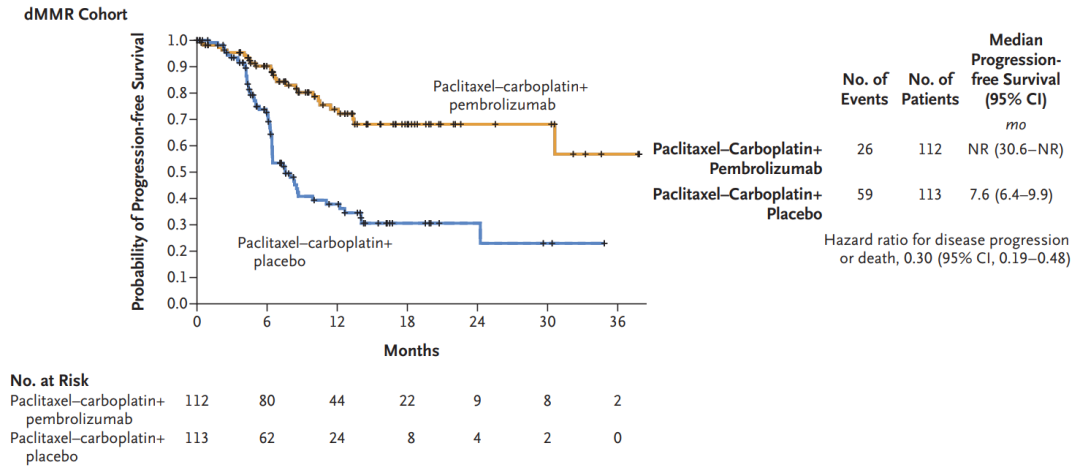
K药新适应症上市申请获FDA受理,一线治疗子宫内膜癌
无论肿瘤的错配修复状态如何,K药联合化疗组患者的PFS均较安慰剂组显著延长。
FDA批准首款CRISPR基因编辑疗法用于治疗第二种疾病——β地中海贫血
Casgevy疗法的获批,并不是旅程的终点,而是一个期待已久的开始。
2023年,FDA发出36份CRL!临床数据缺乏、CMC缺陷占大头
通过对2023年FDA发出的CRL可以发现,临床数据缺陷和CMC问题是影响到药物获批的最主要原因。
司美格鲁肽迎来真正对手!礼来最强减肥药替尔泊肽获FDA批准上市
此次替尔泊肽(Tirzepatide)作为减肥药物获批上市,成为新的“首选减肥药”,华尔街投资银行 Cowen 的分析师认为,替尔泊肽很可能在五年内成为销售额最高的减肥药。