康方生物抗PD1/CTLA4双特异抗体新药AK104 中国临床试验顺利启动,首批患者入组完成!
3月1日,中山康方生物医药有限公司(以下称康方生物)宣布,其旗下子公司康方药业有限公司的抗PD-1/CTLA-4双特异抗体新药AK104 在中国启动Ib/II期临床试验,首批第一队列患者已经在北京肿瘤医院顺利入组和给药。AK104是新一代的抗肿瘤免疫治疗药物,是康方生物利用康方独特的Tetrabody双抗平台、自主研发的首款双抗产品,也是全球首个进入临床试验的PD-1/CTLA-4双特异抗体。这项
上海复宏汉霖利妥昔单抗(汉利康)获批,治疗非霍奇金淋巴瘤
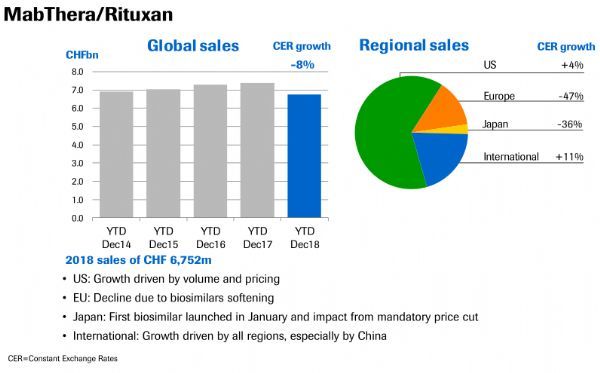
2019年2月26日讯 /生物谷BIOON/ --2月22日,中国国家药品监督管理局(NMPA)批准上海复宏汉霖生物制药有限公司研制的利妥昔单抗注射液(HLX-01,商品名:汉利康)上市注册申请。该药是国内获批的首个生物类似药,主要用于非霍奇金淋巴瘤的治疗。汉利康(HLX-01)是瑞士制药巨头罗氏三大王牌生物制剂之一——MabThera/Rituxan(中文商品名:美罗华,通用名:rituxima
Sobi完成收购阿斯利康呼吸道合包病毒(RSV)药物Synagis和MEDI8897
2019年01月31日讯 /生物谷BIOON/ --瑞典制药公司Swedish Orphan Biovitrum AB(SOBI) 近日宣布,已完成对阿斯利康下呼吸道感染药物Synagis(palivizumab)在美国权益的收购。此外,该公司也有权获得阿斯利康候选药物MEDI8897在美国市场未来收益的50%分成。根据之前签署的协议,与这2个资产相关的130名阿斯利康员工将转移至Sobi。Syn
阿斯利康便秘新药Linzess(利那洛肽)获中国批准,将填补国内治疗空白
2019年1月22日讯 /生物谷BIOON/ --阿斯利康(AstraZeneca)与合作伙伴Ironwood近日宣布,便秘新药Linzess(linaclotide,利那洛肽)已获中国国家药品监督管理局(NMPA)批准,用于便秘型肠易激综合征(IBS-C)成人患者的治疗。阿斯利康表示,这款药物将在2019年下半年在中国上市。在中国,肠易激综合征(IBS)是一种常见的慢性致衰性疾病,IBS-C是其
绿叶制药新搭档:将心血管产品在华独家推广权授予阿斯利康
今晨,阿斯利康中国宣布与绿叶制药集团签署协议,正式宣布获得血脂康胶囊产品在中国大陆地区的独家推广权。而绿叶制药继续持有该药品的资产权、商业销售权、注册准证、全部知识产权等推广权以外的权利。这是大型跨国药企首次在华获权推广由中国药企自主研发的创新中成处方药。在国家推动实施《中医药发展战略规划纲要》的背景下,此举也有助于提升中医药现代化水平和国际竞争力,推动中医药健康产业的升级,并有望助力开拓中医药的
阿斯利康中国与绿叶制药宣布战略合作 深耕心血管领域践行中国承诺
昨日,阿斯利康中国宣布与绿叶制药集团签署协议,正式宣布获得血脂康胶囊产品在中国大陆地区的独家推广权。这是大型跨国药企首次在华获权推广由中国药企自主研发的创新中成处方药。在国家推动实施《中医药发展战略规划纲要》的背景下,此举也有助于提升中医药现代化水平和国际竞争力,推动中医药健康产业的升级,并有望助力开拓中医药的国际化发展道路,让高品质本土中成药惠及广大患者。 昨日,阿斯利康中国宣布与绿
Mayne制药公司在美国市场推出Tolsura(SUBA-伊曲康唑,65mg胶囊)
2019年1月31日讯 /生物谷BIOON/ --澳大利亚生物技术公司Mayne Pharma近日宣布,在美国市场推出Tolsura(SUBA®-itraconazole,SUBA-伊曲康唑)65mg胶囊。在美国,Tolsura于2018年12月获得了FDA批准。Tolsura是一种新的伊曲康唑制剂,用于成人患者治疗系统性真菌感染,包括:芽生菌病(肺和肺外)、组织胞浆菌病(包括慢性空洞性
阿斯利康roxadustat(罗沙司他)2个III期临床获得成功
2018年12月23日讯 /生物谷BIOON/ --英国制药巨头阿斯利康(AstraZeneca)近日宣布,评估新型贫血药物roxadustat(罗沙司他)治疗慢性肾脏病(CKD)患者贫血的2个III期临床研究OLYMPUS(非透析依赖)和ROCKIES(透析依赖)均达到了主要终点。OLYMPUS是一项随机、双盲、安慰剂对照、III期研究,在伴贫血的3、4、5期CKD患者中开展,这些患者病情进展为
阿斯利康/默沙东Lynparza治疗复发性BRCAm晚期卵巢癌III期临床获成功
2018年12月22日讯 /生物谷BIOON/ --英国制药巨头阿斯利康(AstraZeneca)与合作伙伴默沙东(Merck & Co)近日联合宣布,评估靶向抗癌药Lynparza(中文品牌名:利普卓,通用名:olaparib,奥拉帕利片剂)治疗复发性BRCA突变晚期卵巢癌的III期临床研究SOLO-3达到了主要终点。SOLO-3是与美国FDA达成一致意见作为一项上市后的承诺研究而开展的
阿斯利康Lynparza一线维持治疗适应症获美国FDA批准
2018年12月20日讯 /生物谷BIOON/ --英国制药巨头阿斯利康(AstraZeneca)与合作伙伴默沙东(Merck & Co)近日联合宣布,美国食品和药物管理局(FDA)已批准Lynparza(中文品牌名:利普卓,通用名:olaparib,奥拉帕利片剂),作为一种维持疗法,用于接受一线含铂化疗病情处于完全缓解或部分缓解的BRCA突变(BRCAm)晚期卵巢癌患者,具体为:仅FDA